海佑福瑞达乌帕替尼原料药DMF在美国FDA完成备案
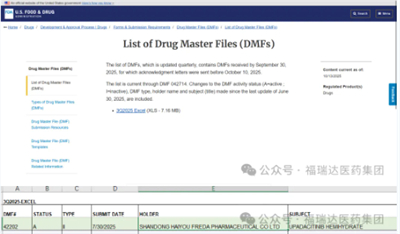
近日,山东海佑福达制药有限公司迎来国际化进程中的里程碑时刻——其自主研发的乌帕替尼半水合物(UPADACITINIB HEMIHYDRATE) 的药品主文件(DMF)于2025年07月30日提交美国食品药品监督管理局(FDA) 并受理,DMF:042202。目前已在FDA平台公示,标志着该原料药已做好供应美国市场的准备,为公司进军全球高端医药市场奠定了坚实基础。
药品主文件(DMF)是制药企业向药品监管机构提交的核心技术文件,详细记载药物活性成分或制剂在生产、加工、包装及储存等环节的关键信息,与制剂申报资料进行关联审评,助力制剂产品在美国成功上市
乌帕替尼作为一种高效选择性JAK1抑制剂,在治疗类风湿关节炎、特应性皮炎等自身免疫性疾病方面显示出显著疗效,市场前景广阔。此次DMF提交,不仅证明了海佑福瑞达制药在原料药研发和生产质量管理体系方面的高标准,也为公司后续产品进军国际市场积累了宝贵经验。
未来,海佑福瑞达将紧密围绕集团原料药战略支撑企业的定位,以技术创新为核心引擎,不断开拓产品更多应用场景的潜力,为国内外客户提供更优质、更具性价比的产品与服务,致力于成为全球医药企业值得信赖的战略合作伙伴。
【特别声明:部分文字及图片来源于网络,仅供学习和交流使用,不具有任何商业用途,其目的在于传递更多的信息,并不代表本平台赞同其观点。版权归原作者所有,如涉版权或来源标注有误,请及时和我们取得联系,我们将迅速处理,谢谢!】















